Hiperandrogenizem jajčnikov. Hiperandrogenizem nadledvične žleze pri ženskah: ključni vidiki bolezni in metode zdravljenja bolezni. Promocije in posebne ponudbe
Patološka manifestacija pri osebi z izrazitimi značilnimi znaki, značilnimi za nasprotni spol, pogosto izzove nadledvični hiperandrogenizem (adrenogenitalni sindrom). Z razvojem tega sindroma v telesu obstaja povečana vsebina androgeni (steroidni moški spolni hormoni), ki vodijo do virilizacije.
Splošne informacije
Virilizacija (maskulinizacija) nadledvične geneze je posledica prekomerne proizvodnje androgenih hormonov s strani nadledvične žleze in vodi do zunanjih in notranjih sprememb, ki so netipične za spol bolnika. Androgeni so bistveni v telesu odrasle ženske, saj so odgovorni za pomembne preobrazbe v telesu med puberteto. Zlasti proizvajajo sintezo estrogena, prispevajo pa tudi k krepitvi kostnega tkiva, rasti mišic, sodelujejo pri uravnavanju jeter in ledvic ter oblikovanju reproduktivnega sistema. Androgene proizvajajo predvsem nadledvične žleze in v žensko telo jajčniki, pri moškem pa moda. Pomemben presežek norme v vsebnosti teh hormonov pri ženskah lahko znatno moti reproduktivni sistem in celo izzove neplodnost.
Vzroki za hiperandrogenizem nadledvične žleze
 Hormonska neravnovesja lahko sprožijo bolezen.
Hormonska neravnovesja lahko sprožijo bolezen. Glavni razlog za kopičenje androgenov v telesu je prirojena okvara v sintezi encimov, ki preprečuje pretvorbo steroidov. Najpogosteje je vloga takšne okvare pomanjkanje C21-hidroksilaze, ki sintetizira glukokortikoide. poleg tega hormonsko neravnovesje je posledica vpliva hiperplazije skorje nadledvične žleze ali tumorjem podobnih tvorb (nekatere vrste nadledvičnih tumorjev so sposobne proizvajati hormone). Najpogosteje diagnosticirana prisotnost nadledvične hiperandrogeničnosti prirojenega tipa. Vendar pa včasih obstajajo primeri hiperandrogenizma zaradi tumorjev nadledvične žleze, ki izločajo androgene (Itsenko-Cushingova bolezen).
Patogeneza
Pomanjkanje C21-hidroksilaze lahko nekaj časa uspešno kompenzirajo nadledvične žleze in preide v dekompenzirano fazo s stresnimi nihanji v hormonskem ozadju, ki nastanejo zaradi čustvenih pretresov in sprememb v reproduktivnem sistemu (začetek spolnih odnosov, nosečnost). Ko postane okvara v sintezi encimov izrazita, se pretvorba androgenov v glukokortikoide ustavi in pride do njihovega prekomernega kopičenja v telesu.
Značilnosti razvoja adrenogenitalnega sindroma pri ženskah
Adrenogenitalni sindrom pri ženskah vodi do resnih sprememb v delovanju jajčnikov in motenj v reproduktivnem sistemu. Po statističnih študijah vsaka peta ženska do neke mere trpi zaradi hiperandrogenizma z različnimi manifestacijami. Poleg tega starost v tem primeru ni pomembna, bolezen se kaže v kateri koli fazi življenski krog začenši od otroštva.
Učinek hiperandrogenizma na delovanje jajčnikov povzroča naslednje manifestacije:
- zaviranje rasti in razvoja foliklov v zgodnji fazi folikulogeneze se kaže z amenorejo (odsotnost menstruacije več ciklov);
- upočasnitev rasti in razvoja folikla in jajčeca, ki ni sposobna ovulacije, se lahko kaže kot anovulacija (pomanjkanje ovulacije) in oligomenoreja (povečanje intervala med menstruacijo);
- ovulacija z okvarjenim rumenim telesom, se izraža v pomanjkanju lutealne faze cikla, tudi ob redni menstruaciji.
Simptomi hiperandrogenizma nadledvične žleze
 Dlake na obrazu pri ženskah se povečajo s hiperandrogenizmom nadledvične žleze.
Dlake na obrazu pri ženskah se povečajo s hiperandrogenizmom nadledvične žleze. Adrenogenitalni sindrom ima primarne in sekundarne manifestacije, odvisno od faze razvoja bolezni in dejavnikov njenega nastanka. Posredni znaki pogosta je prisotnost nadledvične hiperandrogenije pri ženskah prehladi, nagnjenost k depresiji, povečana utrujenost.
Glavni simptomi hiperandrogenizma nadledvične žleze:
- povečana rast linijo las(okončine, trebuh, mlečne žleze), do hirzutizma (rast dlak na licih);
- plešavost s tvorbo plešastih madežev (alopecija);
- napake na koži (akne, akne, luščenje in druga vnetja);
- mišična atrofija, osteoporoza.
Naslednje manifestacije so sekundarni simptomi adrenogenitalnega sindroma:
- arterijska hipertenzija, ki se kaže v obliki napadov;
- povišana raven glukoza v krvi (sladkorna bolezen tipa 2);
- hitro pridobivanje prekomerne telesne teže, vse do debelosti, ki zahteva zdravljenje;
- vmesna vrsta tvorbe ženskih spolnih organov;
- odsotnost menstruacije ali znatni intervali med menstruacijami;
- neplodnost ali spontani splav (za uspešno nosečnost je v telesu potrebna določena količina ženskih hormonov, katerih proizvodnja se v primeru hiperandrogenizma praktično ustavi).
za citiranje: A. A. Pishchulin, E. A. Karpova Hiperandrogenizem jajčnikov in metabolični sindrom // BC. 2001. št.2. str. 93
Endokrinološki znanstveni center RAMS, Moskva
Z indromo hiperandrogenizma jajčnikov netumorske geneze ali hiperandrogene disfunkcije jajčnikov, ki se je prej imenoval Stein-Leventhalov sindrom, danes je po klasifikaciji WHO v svetovni literaturi bolj znan kot sindrom policističnih jajčnikov (SPANJE).
Klinična slika PCOS se kaže s kroničnim anovulacijskim stanjem jajčnikov ali hudo hipofunkcijo rumenega telesa, kar vodi v obojestransko povečanje velikosti jajčnikov z zadebelitvijo in sklerozo tunice albuginea. Te spremembe se kažejo s kršitvijo menstrualne funkcije - opsomenoreja, amenoreja, vendar ni izključen razvoj metroragije. Motnje folikulogeneze vodijo v razvoj anovulacijske primarne ali sekundarne neplodnosti.
Eno glavnih diagnostičnih meril za PCOS je hiperandrogenizem. - zvišanje ravni androgenih steroidov v krvi (kot sta testosteron, androstendion), kar vodi v razvoj hirzutizma in drugih androgeno odvisnih dermopatij.
Debelost ali prekomerna telesna teža je pogosto povezana s PCOS. Določanje indeksa telesne mase (BMI) vam omogoča, da ugotovite stopnjo debelosti. Merjenje kazalnikov volumna pasu (OT) in bokov (OB) ter njihovega razmerja kaže na vrsto debelosti (prognostično neugoden je abdominalni tip debelosti, pri katerem je OT/OB> 0,85).
Poleg glavnih simptomov bolezni klinično sliko v veliki meri določa splošna presnovne motnje kot so dislipidemija, motnja presnova ogljikovih hidratov, povečano tveganje za razvoj hiperplastičnih in neoplastičnih procesov iz genitalij. Dislipidemija je povečanje trigliceridov, holesterola, lipoproteinov nizke gostote, lipoproteinov zelo nizke gostote in zmanjšanje lipoproteinov visoke gostote. Te motnje vodijo v tveganje za zgodnji razvoj aterosklerotičnih žilnih sprememb, hipertenzija in ishemična bolezen srca.
Motnje v presnovi ogljikovih hidratov so sestavljene iz razvoja kompleksa insulinske rezistence-hiperinzulinemije, ki je v zadnjem času postala glavna smer pri preučevanju patogenetskih povezav pri razvoju PCOS.
V 60-ih letih je bila patogeneza PCOS povezana s primarno encimsko okvaro jajčnikov 19-hidroksilaze in/ali 3b-dehidrogenaze, kar je te motnje združilo v koncept primarnega policističnega jajčnika. Vendar pa se je v delih naslednjih let pokazalo, da je aktivnost aromataze granuloznih celic funkcija, odvisna od FSH.
Povečana raven luteinizirajočega hormona (LH), ugotovljena pri PCOS, odsotnost njegovega ovulacijskega vrha, normalna ali zmanjšana raven folikle stimulirajočega hormona (FSH) z oslabljenim razmerjem LH/FSH (2,5-3) so kazali na primarno kršitev gonadotropna regulacija steroidogeneze v tkivu jajčnikov z razvojem sekundarne bolezni policističnih jajčnikov.
Do sredine osemdesetih let prejšnjega stoletja je veljalo (teorija SSC Yen), da je sprožilni mehanizem v patogenezi PCOS prekomerna sinteza androgenov s strani nadledvične žleze med adrenarho kot posledica spremenjene občutljivosti nadledvičnih žlez na ACTH ali prekomerne stimulacije. skorje nadledvične mrežnice zaradi faktorja, ki ni podoben ACTH, ali pod vplivom b-endorfina, nevrotransmiterjev, kot je dopamin. Ob dosegu kritična masa telesu (zlasti, če je njegova norma presežena), se periferna pretvorba androgenov v estrogene poveča, predvsem v jetrih in maščobnem tkivu. Zvišanje ravni estrogenov, predvsem estrona, vodi v preobčutljivost gonadotrofov glede na luliberin (GnRH). Hkrati se pod vplivom estrona poveča proizvodnja GnRH v hipotalamusu, povečata se amplituda in frekvenca njegovih impulzov izločanja, zaradi česar se poveča proizvodnja LH z adenohipofizo, razmerje LH / FSH se poveča. moteno in pride do relativnega pomanjkanja FSH. Krepitev učinka LH na jajčnike prispeva k povečanju proizvodnje androgenov v tekalnih celicah in njihovi hiperplaziji. Relativno nizka stopnja FSH vodi do zmanjšanja aktivnosti od FSH odvisne aromataze, granulozne celice pa izgubijo sposobnost aromataze androgenov v estrogene. Hiperandrogenizem moti normalno rast foliklov in prispeva k nastanku njihove cistične atrezije. Pomanjkanje rasti in zorenja foliklov dodatno zavira izločanje FSH. Povečana količina androgenov v perifernih tkivih se pretvori v estron. Začaran krog se zapre.
Tako je posledica kršitve centralnih in perifernih mehanizmov regulacije steroidogeneze razvoj funkcionalnega hiperandrogenizma jajčnikov pri bolnikih s PCOS.
Patogeneza PCOS po S.S.C. Jen je prikazan na diagramu 1:
Shema 1.
V zgodnjih 80. letih so številni avtorji predlagali novo teorijo patogeneze sindroma policističnih jajčnikov, drugačno od teorije S.S.C. jen. Ugotovljeno je bilo, da je PCOS povezan s hiperinzulinemijo in zanj so značilne tako reproduktivne kot presnovne disfunkcije.
Na obstoj povezave med hiperinzulinemijo in hiperandrogenizmom sta že leta 1921 opozorila Achard in Thieris. Opisali so hiperandrogenizem pri debeli ženski s sladkorno boleznijo tipa 2 in stanje poimenovali "sladkorna bolezen pri bradatih ženskah".
Kasneje je D. Bargen ugotovil, da so imele ženske s PCOS in hiperandrogenizmom bazalno in z glukozo stimulirano hiperinzulinemijo v primerjavi s kontrolno skupino žensk enake teže, kar kaže na prisotnost insulinske rezistence. Obstajala je neposredna povezava med ravnmi insulina in androgena in domnevali so, da bi lahko bila hiperinzulinemija vzrok za hiperandrogenizem.
Leta 1988 je G. Reaven prvič predlagal, da imata IR in kompenzacijska hiperinzulinemija (GI) pomembno vlogo pri razvoju sindroma presnovnih motenj. Poimenoval ga je "sindrom X" ... Trenutno je najpogosteje uporabljen izraz "metabolični sindrom" ali "sindrom inzulinske rezistence".
Hipoteze o patogenezi hiperinzulinemije in hiperandrogenizma Mehanizem pojava hiperandrogenizma in hiperinzulinemije ni popolnoma razumljen. Teoretično so možne tri interakcije: hiperandrogenizem (GA) povzroča GI; GI vodi v GA: obstaja tretji dejavnik, ki je odgovoren za oba pojava.
1. Domneva, da GA povzroča GI, temelji na naslednjih dejstvih. Pri ženskah, ki jemljejo peroralne kontraceptive, ki vsebujejo progestine z "androgenimi lastnostmi", najdemo oslabljeno toleranco za glukozo. Dolgotrajno predpisovanje testosterona transseksualcem spremlja pojav IR. Dokazano je, da androgeni vplivajo na sestavo mišičnega tkiva s povečanjem števila mišičnih vlaken druge vrste, ki so manj občutljiva na inzulin v primerjavi z vlakni prve vrste.
2. Večina dejavnikov kaže, da GI vodi v GA. Pokazalo se je, da IR vztraja pri bolnicah, pri katerih je bila izvedena subtotalna ali popolna odstranitev jajčnikov, pa tudi pri ženskah, ki so dolgo uporabljale agoniste GnRH, ko je prišlo do izrazite supresije ravni androgena. Dajanje diazoksida, zdravila, ki zavira izločanje inzulina s strani trebušne slinavke, je povzročilo znižanje ravni testosterona (T) in povečanje ravni globulina, ki veže spolne steroide (SSSH) pri bolnikih s PCOS, debelostjo in hiperinzulinemijo. Intravenska uporaba inzulin pri ženskah s PCOS je povzročil zvišanje ravni androstenediona in T v obtoku. Intervencije za povečanje občutljivosti za inzulin (izguba teže, post in nizkokalorična dieta) je spremljalo znižanje ravni androgenov. Obstajajo dokazi, da lahko insulin neposredno zavira nastajanje CCH v jetrih, v pogojih hiperinzulinemije pa se ta učinek poveča. Hkrati se verjame, da je insulin in ne spolni hormoni glavni regulator sinteze CCSS. Zmanjšanje ravni SHSS vodi do povečanja koncentracije prostega in zato biološko aktivnega T (običajno je 98% T v vezanem stanju).
Hipoteza, ki povezuje HA s hiperinzulinemijo, ne odgovarja na vprašanje, kako jajčnik ohranja občutljivost za inzulin, ko je telo odporno na inzulin. Predlaganih je več možnih razlag. Ker ima inzulin veliko funkcij, lahko domnevamo selektivno okvaro nekaterih od njih. Občutljivost na inzulin je lahko organsko specifična. Vendar je bolj verjetno, da insulin na jajčnik ne deluje samo prek insulinskih receptorjev, temveč tudi prek receptorjev za insulinu podobne rastne faktorje (IGF).
Inzulinske receptorje in receptorje IGF-1 so identificirali v človeških jajčnikih (v stromalnem tkivu jajčnikov zdravih žensk, žensk s PCOS, v folikularnem tkivu in granuloznih celicah). Inzulin se lahko veže na receptorje IGF-1, čeprav z manjšo afiniteto kot njegovi lastni receptorji. Vendar pa je pri GI, pa tudi v situaciji, ko so insulinski receptorji blokirani ali pomanjkljivi, lahko pričakujemo, da se bo insulin v večji meri vezal na receptorje IGF-1.
Morda lahko mehanizme stimulacije steroidogeneze inzulina / IGF-1 v jajčniku razdelimo na nespecifične in specifične. Nespecifični so klasični učinki insulina na glukozo, presnovo aminokislin in sintezo DNK. Posledično se poveča sposobnost preživetja celice in posledično se poveča sinteza hormonov. Posebni mehanizmi vključujejo neposredno delovanje insulin/IGF-1 na steroidogene encime, sinergizem med insulinom in LH/FSH ter učinki na število LH receptorjev.
Insulin/IGF-1, ki deluje sinergistično s FSH, stimulira aktivnost aromataze v kulturi granuloznih celic in s tem poveča sintezo estradiola. Poleg tega vodijo do povečanja koncentracije LH receptorjev, kar poveča sintezo androstendiona, odvisno od LH, s teka in stromalnimi celicami.
Povečana koncentracija androgenov v jajčniku pod delovanjem insulina/IGF-1 povzroči folikularno atrezijo, ki vodi v postopno izločanje granuloznih celic, ki proizvajajo estrogen in progesteron, čemur sledi hiperplazija tekalnih celic in luteinizacija intersticijskega tkiva. jajčnika, ki je mesto proizvodnje androgenov. To pojasnjuje dejstvo, da se stimulacija steroidogeneze jajčnikov z insulinom kaže predvsem v obliki hiperandrogenizma.
Domneva se, da lahko insulin/IGF-1 stimulira tako LH odvisno aktivnost citokroma P450c17a v jajčnikih kot ACTH odvisno aktivnost P450c17a v nadledvičnih žlezah. To očitno pojasnjuje pogosto kombinacijo hiperandrogenizma jajčnikov in nadledvične žleze pri bolnikih s PCOS.
Možna je tudi povezava s S.S.C. Jen o vpletenosti nadledvične steroidogeneze v patogenezo PCOS (shema 2).

Shema 2. Delovanje insulina pri sindromu policističnih jajčnikov
V. Insler (1993), ki je opravil študijo ravni insulina, IGF-1, rastnega hormona in njihove korelacije z nivoji gonadotropinov in androgenov pri ženskah s PCOS, je predlagal dva modela za razvoj tega sindroma. Pri debelih bolnikih GI inducira prekomerno proizvodnjo androgenov preko receptorjev IGF-1, ki v sinergiji z LH povzročijo povečanje aktivnosti citokroma P450c17a, glavnega nadzornega encima pri sintezi androgena. Pri bolnikih z normalno telesno težo relativno povečanje koncentracije rastnega hormona spodbuja prekomerno proizvodnjo IGF-1. Od tega trenutka naprej sinergizem z LH vodi do prekomerne proizvodnje androgena po enakem mehanizmu kot pri debelih bolnikih. Povečanje ravni androgenov povzroči spremembo delovanja hipotalamičnih centrov, kar vodi do kršitve izločanja gonadotropinov in sprememb, značilnih za PCOS (shema 3).
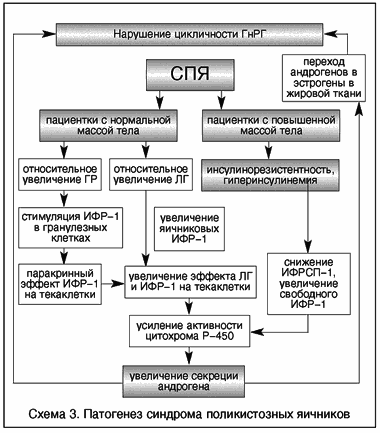
Shema 3. Patogeneza sindroma policističnih jajčnikov
3. Vendar pa obstajajo številna dobro znana stanja IR, ki niso povezana z GA, kot sta preprosta debelost in sladkorna bolezen tipa 2. Da bi pojasnili, zakaj vsi debeli bolniki z GI ne razvijejo hiperandrogenizem in PCOS, postavil hipotezo o obstoju genetske nagnjenosti k stimulativnemu učinku insulina na sintezo androgenov v jajčniku ... Očitno obstaja gen ali skupina genov, zaradi katerih so jajčniki ženske s PCOS bolj občutljivi na inzulinsko stimulacijo proizvodnje androgena.Molekularni mehanizmi, ki vodijo do razvoja insulinske rezistence, niso popolnoma razumljeni. Vendar pa je nedavni napredek v molekularni biologiji omogočil določitev strukture gena, ki kodira insulinski receptor pri ženskah s hiperandrogenizmom jajčnikov.
Moller in Flier sta proučevala zaporedje aminokislin v strukturi verig DNK pri bolnicah s hiperandrogenizmom jajčnikov. Odkrili so zamenjavo triptofana za serozin pri kodonu 1200. Raziskovalci so predlagali, da taka sprememba moti aktivacijo tirozin kinaznega sistema v insulinskem receptorju. Nizka aktivnost insulinskih receptorjev vodi do razvoja IR in kompenzacijskega GI.
Yoshimasa et al. opisal drugo varianto točkovne mutacije pri bolniku s hiperandrogenizmom, inzulinsko rezistenco in acanthosis nigricans. Odkrili so zamenjavo serina za arginin v tetramerni strukturi inzulinskega receptorja. Ta mutacija v aktivnem lokusu je onemogočila povezavo a- in b-podenot, zaradi česar ni bil sintetiziran funkcionalno aktiven receptor. Zgornje študije so le prvi poskusi identifikacije specifične genetske etiologije stromalne tekomatoze jajčnikov.
Pozneje Dunaif A. ugotavlja, da lahko pri sindromu policističnih jajčnikov IR povzroči motena avtofosforilacija b-podenot inzulinskega receptorja (IR), katerega citoplazemski del ima aktivnost tirozin kinaze. Hkrati se z zatiranjem aktivnosti tirozin kinaze (sekundarni signalni oddajnik, ki določa občutljivost insulina na receptorje z istim imenom) poveča inzulinsko neodvisna fosforilacija serinskih ostankov (PCOS-ser). Ta okvara je značilna samo za PCOS-odvisno IR, pri drugih inzulinsko odpornih stanjih (debelost, NIDDM) teh sprememb ne zaznamo.
Ni mogoče izključiti, da v PCOS-ser obstaja določen serinski fosforilacijski faktor. Tako je na primer izoliran inhibitor serin / treonin fosfataze, ki očitno moti fosforilacijo IR v PCOS-ser. Ta spojina je podobna nedavno izoliranemu membranskemu glikoproteinu PC-1 (zaviralec insulinske receptorske tirozin kinaze), vendar slednji ne poveča od insulina neodvisne fosforilacije serinskega IR.
Faktor tumorske nekroze-a (TNF-a) ima podobne lastnosti: fosforilacija serinskih ostankov IRS-1 (eden od sekundarnih prenašalcev IR signala) pod vplivom TNF-a povzroči zatiranje aktivnosti tirozin kinaze IR.
Moller et al. ugotovili, da fosforilacija humanega serina P450c17, ključnega encima, ki uravnava biosintezo androgenov nadledvične žleze in jajčnikov, poveča aktivnost 17,20-liaze. Modulacija encimske aktivnosti steroidogeneze s fosforilacijo serina je bila opisana za 17b-hidroksisteroid dehidrogenazo. Če predpostavimo, da isti faktor (encim) fosforilira serin inzulinskega receptorja, ki povzroča IR, in P450c17 serin, ki povzroča hiperandrogenizem, potem je mogoče razložiti razmerje med PCOS in IR. Poskusi in vitro so pokazali, da protein kinaza A (serin/treonin kinaza) katalizira fosforilacijo serina inzulinskih receptorjev (shema 4).

Shema 4. Gen insulinske rezistence pri PCOS
Vloga leptina pri PCOSV zadnjem času so bile izvedene številne študije o biološka vloga leptin, katerega rezultati so spodbudni. Kot beljakovinski hormon leptin vpliva na prehranjevalno vedenje in ima dovoljen učinek na začetek pubertete pri živalih. Vloga tega hormona pri uravnavanju presnove in reproduktivne funkcije pri človeku žal ni povsem razjasnjena. Zato so podatki o ravni leptina pri hiperandrogenizmu jajčnikov v kombinaciji z inzulinsko rezistenco in koncept njegove vloge pri razvoju teh sprememb zelo protislovni.
V zadnjem času so se pojavile številne študije o biološki vlogi leptina, katerih rezultati so spodbudni. Kot beljakovinski hormon leptin vpliva na prehranjevalno vedenje in ima dovoljen učinek na začetek pubertete pri živalih. Vloga tega hormona pri uravnavanju presnove in reproduktivne funkcije pri človeku žal ni povsem razjasnjena. Zato so podatki o ravni leptina pri hiperandrogenizmu jajčnikov v kombinaciji z inzulinsko rezistenco in koncept njegove vloge pri razvoju teh sprememb zelo protislovni.Tako je po študiji Brzechffa et al. (1996), ima pomemben delež žensk v populaciji s PCOS višje ravni leptina od pričakovane glede na njihov ITM, prosti testosteron in občutljivost za inzulin. Po drugi strani pa zadnje delo na tem področju ni pokazalo pomembnih razlik v ravneh leptina v študijskih skupinah s PCOS in v kontrolnih skupinah. Poleg tega je bilo ugotovljeno, da bazalna raven inzulina, vsebnost gonadotropinov in spolnih steroidov ne vplivajo na vsebnost leptina. Vendar sta Zachow in Magffin (1997) ob upoštevanju podatkov o prisotnosti mRNA receptorjev za leptin v tkivu jajčnikov pokazala neposreden učinek tega hormona na steroidogenezo granuloznih celic podgan in vitro. Hkrati se je izkazal od odmerka odvisen supresivni učinek leptina na IGF-1, potenciran s povečanjem FSH-stimulirane sinteze E 2 v granuloznih celicah. Ti podatki podpirajo hipotezo, da lahko povišane ravni leptina pri debelih posameznikih preprečijo zorenje. prevladujoči folikel in ovulacijo. Zelo zanimivi so podatki Spicer in Franciso (1997), ki kažejo, da leptin v naraščajočih koncentracijah (10-300 ng/ml) zavira inzulinsko odvisno proizvodnjo E 2 in progesterona v kulturi granuloznih celic. Ta učinek je posledica prisotnosti specifičnih veznih mest za leptin. Po analogiji s tem je mogoče domnevati, da visoka stopnja leptin lahko zmanjša občutljivost drugih ciljnih tkiv na delovanje endogenega inzulina, kar vodi do razvoja IR pri debelosti.
Diagnoza Diagnostika sindroma hiperandrogenizma jajčnikov s tipično klinična slika ni težko. Najprej gre za kršitev menstrualne funkcije po vrsti oligo-, opso- ali amenoreje, anovulacijo in posledično primarno ali sekundarno neplodnost, hirzutizem, akne, 40% bolnikov ima debelost različne resnosti. Ginekološki pregled razkrije obojestransko povečanje velikosti jajčnikov, pogosto v ozadju hipoplastične maternice.
Hormonske raziskovalne metode igrajo pomembno vlogo pri diagnozi PCOS. , namenjen ugotavljanju hiperandrogenizma, njegovega vira in določanju ravni gonadotropnih hormonov: LH in FSH. Bolniki s PCOS imajo pogosto prevlado ravni LH nad FSH, njihovo razmerje je poslabšano in povečano (več kot 2,5-3). Raven prolaktina je normalna, čeprav se pri 30% bolnikov opazi nekaj povečanja.
Stopnja izločanja skupnega 17-KS z urinom pri PCOS se zelo razlikuje in ni zelo informativna. Določitev frakcij 17-KS (DHA, 11-oksidirani ketosteroidi, androsteron, etioholanolon) tudi ne omogoča identifikacije lokalizacije vira hiperandrogenizma. Potrditev vira hiperandrogenizma jajčnikov je zvišanje ravni androstendiona (A) in testosterona (T) v krvi ter povečanje razmerja A / T. Nadledvična geneza hiperandrogenizma je potrjena s povečanjem ravni dehidroepiandrosterona (DHA) in njegovega sulfata (DHA-S) ter 17-hidroksiprogesterona (17-OH-R) v krvi. Za razjasnitev lokalizacije vira hiperandrogenizma so bili predlagani različni funkcionalni testi, med katerimi je najpogostejši test z deksametazonom, synacthen-depo.
Ob upoštevanju odkritja novih patogenetskih povezav pri razvoju PCOS je za oceno stanja presnove ogljikovih hidratov potrebno izvesti standardni glukoznotolerancni test (75 ml glukoze per os) z določitvijo glukoze in imunoreaktivnega ravni insulina (IRI). Dokazi v prid odpornosti proti insulinu so tudi ITM nad 25 in OT/OB nad 0,85 ter dislipidemija.
Zdravljenje V središču sodoben pristop na patogenetsko zdravljenje PCOS načelo obnove okvarjenega delovanja jajčnikov
, to je odprava anovulacije, kar posledično vodi do zmanjšanja hiperandrogenizma in obnove folikulogeneze. Vendar pa študija značilnosti etiopatogeneze hiperandrogenizma jajčnikov vodi do zaključka, da izbira metod ustreznega zdravljenja PCOS ni lahka naloga.
Kombinirani peroralni kontraceptivi je najpogosteje uporabljena skupina zdravil za PCOS. Mehanizem delovanja je zatiranje povišanega LH, normalizacija razmerja LH/FSH in povečanje sinteze CCH v jetrih. Po preklicu se doseže "rebound učinek", ki je sestavljen iz normalizacije hipotalamično-hipofizne funkcije, zmanjšanja prekomerne proizvodnje androgenov v tkivu jajčnikov, normalizacije folikulogeneze in ponovne vzpostavitve ovulacije.
Zdravljenje poteka po standardni shemi: 1 tableta na dan od 5 do 25 dni cikla 3-6 mesecev. Po potrebi se tečaji ponovijo. Vendar pa je znano, da lahko dolgotrajna uporaba estrogensko-progestogenih kontraceptivov povzroči hiperinzulinemijo in s tem poslabša glavno patogenetsko povezavo pri PCOS.
Nekatera kontracepcijska sredstva vsebujejo progestogene sestavine, derivate 19-norsteroidov (noretisteron, levonorgestrel), ki imajo različne stopnje androgenih učinkov, zato je predpisovanje zdravil, ki vsebujejo te sestavine, pri bolnikih s hirzutizmom omejeno. Za simptome hiperandrogenizma je bolj priporočljiva uporaba peroralnih kontraceptivov z gestagenom brez androgenega delovanja.
Morda uporaba gestagenih zdravil brez androgenih lastnosti v obliki monoterapije, zlasti pri hiperplaziji endometrija. Didrogesteron je predpisan 1 tableta (10 mg) 2-krat na dan od 14-16 do 25 dni cikla, ki traja od 3 do 6 tečajev.
Najučinkovitejši način za spodbujanje ovulacije pri PCOS je antiestrogensko zdravilo klomifen citrat ... Glavni učinki antiestrogenov so zmanjšanje preobčutljivosti hipofize na delovanje GnRH, zmanjšanje proizvodnje LH, indukcija ovulacijskega sproščanja LH in stimulacija ovulacije. Zdravilo je predpisano v odmerku 50 mg, 100 mg na dan od 5 do 9 dni cikla do ovulacije glede na teste funkcionalne diagnostike, vendar ne več kot 3 tečaje zapored. Nedavno so se pojavile publikacije o učinku klomifen citrata na inzulinu inzulinu podoben rastni faktor. Navedli so, da je bilo do 5. dne stimulacije ovulacije s klomifenom (150 mg / dan) ugotovljeno progresivno znižanje (za največ 30%) ravni IGF-1. Vendar pa v številnih drugih podobnih študijah niso ugotovili pomembnega zmanjšanja bazalnih ravni insulina kot odziv na uvedbo klomifena.
Pojav zdravil z antiandrogenimi lastnostmi je znatno razširil terapevtske možnosti za PCOS. Najbolj razširjeno zdravilo je Diane-35, ki vsebuje 35 mg etinilestradiola in 2 mg ciproteron acetata. Poleg delovanja, značilnega za peroralne kontraceptive, zdravilo blokira delovanje androgenov na ravni ciljnih celic, zlasti lasnih mešičkov. Slednje vodi do zmanjšanja hirzutizma. Zdravilo se uporablja po standardni shemi kot peroralni kontraceptiv v tečajih 6 ali več ciklov. Vendar je treba opozoriti na prisotnost negativnega učinka teh zdravil na presnovo lipidov in ogljikovih hidratov, ki se kaže v zvišanju holesterola, ravni lipoproteinov nizke gostote, pa tudi v povečanju hiperinzulinemije, kar zahteva stalno dinamično spremljanje teh parametrov pri bolnikih s PCOS. Antiandrogene lastnosti ima tudi spironolakton, ki se pogosto uporablja pri zdravljenju androgen odvisnih dermopatij.
Ena od glavnih smeri v sodobna terapija hiperandrogenizem jajčnikov je iskanje in uporaba zdravil in sredstev za odpravo insulinske rezistence in kompenzacijske hiperinzulinemije.
Najprej so to ukrepi, ki zagotavljajo zmanjšanje odvečne telesne teže: nizkokalorična prehrana (v območju 1500-2200 kcal / dan) z omejevanjem maščob in lahko prebavljivih ogljikovih hidratov, omejevanjem vnosa soli na 3-5 g na dan, zmerna telesna aktivnost, normalizacija delovnega režima in počitek. Možna je uporaba zdravil, ki pomagajo zmanjšati ITM, na primer orlistat, ki selektivno zavira gastrointestinalne lipaze ("blokator maščob"), ali sibutramin, ki blokira ponovni privzem noradrenalina in serotonina v sinapsah centra za nasičenost hipotalamusa. Povečana poraba energije (termogeneza) je tudi posledica sinergijske interakcije med okrepljeno funkcijo noradrenalina in serotonina v centralnem živčnem sistemu. To se odraža v selektivni aktivaciji centrale simpatični vpliv na rjavem maščobnem tkivu zaradi posredne aktivacije b 3 -adrenergičnih receptorjev.
Naslednji korak je uporaba zdravil, ki izboljšajo oslabljeno občutljivost tkiv na delovanje insulina. V literaturi obstajajo dokazi o zmanjšanju hiperandrogenizma in obnovi menstrualne in ovulacijske funkcije pri predpisovanju zdravil številnih bigvanidov (Metformin / Siofor® /, Berlin-Chemi). Potencirajo delovanje insulina na receptorski in postreceptorski ravni ter bistveno izboljšajo občutljivost tkiv na ta hormon. Nekatere študije so pokazale znatno zmanjšanje ravni insulina na tešče in 2 uri po obremenitvi s 75 g glukoze pri ženskah s PCOS, ki so uporabljale metformin. To zmanjšanje je bilo povezano z zmanjšanjem ravni androgenov. Opozoriti je treba tudi, da uporaba bigvanidov, ki normalizirajo motnje ogljikovih hidratov, pogosto vodi do zmanjšanja ITM pri debelih bolnikih in pozitivno vpliva na presnovo lipidov.
Svetovna literatura poroča o rezultatih uporabe zdravil, ki spadajo v razred tiazolidindionov. Študije so pokazale, da med zdravljenjem troglitazon (200-400 mg / dan) izboljša občutljivost na insulin pri ženskah s PCOS in zmanjša raven androgenov. Vendar pa odkrit citotoksični, hepatotoksični učinek te skupine zdravil omejuje možnost njihove široke uporabe. V teku je iskanje novih zdravil, ki selektivno vplivajo na občutljivost za inzulin.
Kljub velikemu arzenalu različnih zdravil, ki se uporabljajo za zdravljenje hiperandrogenizma jajčnikov, mora biti zdravljenje te patologije celovito in dosledno, ob upoštevanju vodilne patogenetske povezave na tej stopnji zdravljenja.
Zdravljenje žensk s PCOS mora biti usmerjeno ne le v odpravo ugotovljenih simptomov te bolezni, temveč tudi v preprečevanje morebitnih prihodnjih zapletov. Zelo pomembno je zatreti prekomerno izločanje androgenov in spodbuditi stabilnost mesečnih menstrualnih krvavitev, kar je uspešno doseženo z uporabo zdravil z antiandrogenimi lastnostmi (Diane-35).
V primeru neučinkovitosti konzervativna terapija po enem letu lahko postavite vprašanje o kirurško zdravljenje - laparoskopija s klinasto resekcijo jajčnikov ali njihovo lasersko vaporizacijo ... Učinkovitost kirurško zdravljenje visoka (do 90-95% okrevanja ovulacije) in predhodna patogenetsko terapijo poveča stabilnost doseženega rezultata.
Literatura:1. Ovsyannikova T.V., Demidova I.Yu., Glazkova O.I. Problemi razmnoževanja, 1998; 6: 5-8.
2. Ginzburg M.M., Kozupitsa G.S. Endokrinološki problemi, 1997; 6: 40-2.
3. Starkova N.T. Klinična endokrinologija. Vodnik za zdravnike, 1991; 399.
4. Givens J.R., Wiedeme E. Ravni B-endorfina in B-lipotropina pri hirsute ženskah: korelacija s telesno težo. J Clin Endocr Metabol. 1980; 50: 975-81.
5. Aleem F.A., McIntosh T. Povišane plazemske ravni f-endorfa v skupini žensk s policistično boleznijo jajčnikov. Fertil in Steril. 1984; 42: 686-9.
6. Dedov I.I., Suntsov Yu.I., Kudryakova S.V. Endokrinološke težave. 1998; 6: 45-8.
7. Francis S., Greenspan, Forshman P.H. Osnovna in klinična endokrinologija. 1987.
8. Akmaev I.K. Endokrinološke težave. 1990; 12-8.
9. Barbieri R.L., Hornstein M.D. Hiperinzulinemija in hiperandrogenizem jajčnikov: vzrok in posledica. Endocrinol Metab Clin North Am. 1988; 17: 685-97.
10. Barbieri R.L., Macris A., Ryan K.J. Inzulin spodbuja kopičenje androgenov pri inkubaciji človeške strome jajčnikov in teke. Ginekološka porodnišnica. 1984; 64: 73-80.
11. Barbieri R.L., Ryan K.J. Hiperandrogenizem, insulinska rezistenca, acantosis nigricans: pogosta endokrinopatija z edinstvenimi patofiziološkimi značilnostmi. Am J Obstet Gynecol. 1983; 147: 90-103.
12. Barbieri R.L., Smith S., Ryan K.J. Vloga hiperinzulinemije v patogenezi hiperandrogenizma jajčnikov. Fertil in Steril. 1988; 50: 197-210.
13. Stuart C.A., Prince M.J., Peters E.J. Ginekola porodnišnice. 1987; 69: 921-3.
14. Jen S.S.C. Kronična anovulacija, ki jo povzročajo periferne endokrine motnje. V: Yen S.S.C., Jaffe R.B. Reproduktivna endokrinologija: fiziologija, patofiziologija in klinično vodenje. Philadelphia: Saunders W.B. 1986; 462-87.
15. Moller D.E., Flier J.S. Odkrivanje spremembe gena inzulinskega reseptorja pri pacientki z insulinsko rezistenco, črno akantozo in sindromom policističnih jajčnikov. N Engl J Med. 1988; 319: 1526-32.
16. Burgen G.A., Givens J.R. Inzulinska rezistenca in hiperandrogenizem: klinični sindromi in možni mehanizmi. Hemisphera Pablishing CO, Washington, DC. 1988; 293-317.
17. Speroff L., Glass R. H. Klinična ginekologija. Endokrinologija in neplodnost 5. izd. 1994.
18. Yoshimasa Y., Seino S., et al. Sladkorna bolezen inzulinske rezistence zaradi točkovne mutacije, ki onemogoča obdelavo insulinskih proreceptorjev./ Znanost. 1988; 240: 784-9.
19. Dunaif A. Endokrin. Rev. 18 (6): 1997; 12: 774-800.
Etinilestradiol + ciproteron acetat
Diane-35 (trgovsko ime)
(Shering AG)
Hiperandrogenizem je endokrina bolezen, ki jo povzroča povečano izločanje moških spolnih hormonov v ženskem telesu. Androgene proizvajajo jajčniki in skorja nadledvične žleze. Odvisno od primarni vzrok patologije se lahko razlikujejo klinični simptomi.
Hiperandrogenizem pri ženskah povzroči povečano izločanje luteinizirajočega hormona v hipofizi, ki blokira sproščanje folikle stimulirajočega hormona in estradiola. Posledično je moten proces zorenja folikla, ne pride do sproščanja jajčeca (anovulacija). Visoke ravni androgenov prispevajo k nastanku več cist v jajčnikih (sindrom policističnih jajčnikov).
Moški hormoni zmanjšajo občutljivost perifernih tkiv za inzulin, kar vodi v zvišanje ravni glukoze v krvi, moteno toleranco za glukozo, presnovo ogljikovih hidratov in razvoj sladkorne bolezni tipa 2.
Razvrsti pravi in idiopatski hiperandrogenizem. V prvem primeru se poveča raven androgenov v krvi ženske, v drugem pa se poveča občutljivost perifernih tkivnih receptorjev na moške hormone.
Vzroki za patologijo
Kaj je hiperandrogenizem in zakaj se pojavi? Glavni vzroki bolezni so:
- tumorji, metastaze nadledvičnih žlez;
- kršitev regulacije hipotalamus-hipofize zaradi travme, tumorjev, vnetnih bolezni možganov;
- tumorji jajčnikov: luteoma, tekoma;
- androgenitalni sindrom je prirojena nepravilnost skorje nadledvične žleze, pri kateri pride do povečane proizvodnje testosterona.

Pri ženskah vzroki za hiperandrogenizem povzročajo kršitev hormonskega ravnovesja, delovanja reproduktivnega sistema, presnovnih procesov v telesu.
Simptomi hiperandrogenizma jajčnikov
Bolezen je ovarijske in nadledvične geneze – odvisno od organa, ki začne intenzivno proizvajati androgene. Hiperandrogenizem jajčnikov se v večini primerov razvije v ozadju sindroma policističnih jajčnikov, manj pogosto tumorji, ki proizvajajo hormone, povzročajo patologijo.
Za PCOS je značilna motnja menstrualni ciklus, neplodnost, zvišane ravni androgenov v krvi. Dekliška postava se spreminja glede na moški tip, lasje na obrazu in telesu začnejo rasti, obseg pasu in prsnega koša se poveča, maščobna plast se odlaga v spodnjem delu trebuha. Delo žlez lojnic je moteno, pojavi se seboreja, akne, ki se ne odzivajo na zdravljenje. Na koži stegen, zadnjice se pojavijo strije. Apneja v spanju(zadrževanje diha) vodi v nespečnost.
Na fotografiji je ženska s značilne lastnosti hirzutizem.

Značilni simptomi hiperandrogenizma pri PCOS so pojav predmenstrualnega sindroma. Ženske postanejo razdražljive, njihovo razpoloženje se pogosto spreminja, migrenske skrbi, intenzivne bolečine v spodnjem delu trebuha, otekanje, bolečina v mlečnih žlezah.
Jajčniki se povečajo 2-3 krat, njihova kapsula se zgosti. V notranjosti organa, več cistične formacije... Hormonsko neravnovesje povzroči zadebelitev in hiperplazijo endometrija maternice, menstruacija postane daljša, obilnejša, s sproščanjem krvnih strdkov.
Simptomi hiperandrogenizma nadledvične žleze
Ta vrsta virilizacije se razvije v ozadju androgenitalnega sindroma. Je podedovana motnja, ki povzroča povečano izločanje androgenov v skorji nadledvične žleze. Prirojeno pomanjkanje organskih encimov do določene točke telo kompenzira, vendar pod vplivom številnih dejavnikov pride do hormonskega neravnovesja. Nosečnost lahko izzove takšno stanje, hud stres, začetek spolne aktivnosti.

Vzrok za hiperandrogenizem nadledvične žleze so lahko tumorji, ki proizvajajo hormone, Itsenko-Cushingova bolezen, hiperprolaktinemija, akromegalija. Rakave celice v retikularni skorji proizvajajo "šibke" androgene. V procesu presnove se moški hormoni spremenijo v bolj aktivno obliko in spremenijo splošno hormonsko ozadje ženske. Debelost pomaga pospešiti te procese.
Hiperandrogenizem nadledvične žleze povzroča ciklične motnje v jajčnikih zaradi zvišanja ravni estrogena, zavira se rast in zorenje folikla, moten je menstrualni ciklus in menstruacija lahko popolnoma preneha. Proces ovulacije ne pride, ženska ne more zanositi in nositi otroka.

Simptomi hiperandrogenizma nadledvične žleze pri deklicah:
- deformacija zunanjih genitalij ob rojstvu, težko je določiti spol otroka (ženski hermafroditizem);
- zapoznel spolni razvoj, menarha se začne pri 15-16 letih, menstrualni ciklus je nepravilen, spremlja ga obilna izguba krvi;
- pri mladostnikih opazimo znake hirzutizma: lasje rastejo na obrazu in telesu kot pri moških;
- akne, seboreja, pigmentacija kože;
- delna atrofija mlečnih žlez;
- povečanje velikosti klitorisa;
- alopecija - izpadanje las na glavi;
- slika se spreminja: ozki boki, široka ramena, nizka rast;
- grob glas.

Pri ženskah v rodni dobi hiperandrogenizem nadledvične žleze vodi do zgodnje prekinitve nosečnosti. To je posledica prenehanja rasti maternice zaradi nastanka okvarjenega rumenega telesa. Večina deklet ima popolnoma moteno menstrualno in porodno funkcijo, razvije se neplodnost, poveča se spolna želja. Hirzutizem je slabo izražen, postava se ne spremeni, presnovni procesi niso moteni.
Mešani tip hiperandrogenizma
Hiperandrogenizem mešane geneze se kaže s simptomi jajčnikov in nadledvične oblike bolezni. Ženske imajo policistične jajčnike in znake androgenitalnega sindroma.
Manifestacije mešane vrste bolezni:
- akne;
- strije;
- povečala krvni pritisk;
- kršitev menstrualnega cikla, amenoreja;
- ciste v jajčnikih;
- neplodnost, zgodnja prekinitev nosečnosti;
- oslabljena toleranca za glukozo ali visok krvni sladkor;
- povečana vsebnost lipoproteinov nizke gostote.

Hiperandrogenizem lahko povzročijo sistemske bolezni, ki prizadenejo skorjo nadledvične žleze, jajčnike ali možgane in motijo presnovo. To so adenomi hipofize, anoreksija nervoza, shizofrenija, sladkorna bolezen 2 vrsti, akromegalija, prolaktinom.
Periferna in centralna hiperandroegnija
S porazom centralne živčni sistem, vnetne, nalezljive bolezni ali zastrupitve telesa, se lahko zavira izločanje gonadotropnih hormonov hipofize, ki so odgovorni za nastajanje luteinizirajočih in folikle stimulirajočih hormonov. Posledično je moten proces zorenja folikla v jajčniku in sinteza spolnih hormonov ter povečana proizvodnja androgenov.
Pri ženskah se odkrijejo simptomi policistične bolezni, disfunkcije jajčnikov, menstrualne motnje, kožni izpuščaji, PMS.

Periferni hiperandrogenizem je posledica povečane aktivnosti kožnega encima, 5-α-reduktaze žlez lojnic, ki pretvori testosteron v bolj aktivni androgen dihidrotestosteron. To vodi v hirzutizem različne resnosti, pojav vulgarnih aken.
Hiperandrogenizem med nosečnostjo
Pri nosečnicah je povečanje ravni androgenov vzrok za spontani splav. Najbolj nevarna obdobja so prvih 7-8 in 28-30 tednov. Pri 40% bolnic opazimo intrauterino hipoksijo ploda, najpogosteje v tretjem trimesečju. Drug zaplet je pozna toksikoza, medtem ko se delovanje ledvic poslabša, krvni tlak se dvigne, pojavi se telesni edem.
Hiperandrogenizem med nosečnostjo lahko privede do prezgodnjega odvajanja amnijske tekočine, zapletenega poroda. Spremembe v hormonskem ozadju negativno vplivajo na razvoj otroka, možganska cirkulacija je lahko motena pri dojenčkih, obstajajo znaki intrauterine podhranjenosti.

Hiperandrogenizem in nosečnost sta razloga za nujno hormonsko terapijo za preprečevanje splava in drugih zapletov. Ženske, ki so že imele spontane splave, splav, povišane ravni moških hormonov, je treba v fazi načrtovanja nosečnosti opraviti temeljit pregled.
Diagnoza bolezni
Diagnoza - hiperandrogenizem se postavi na podlagi rezultatov laboratorijskih preiskav na raven hormonov. S sindromom policističnih jajčnikov v krvi ženske se poveča raven testosterona, androstendiona in luteinizirajočega hormona. Koncentracija FSH, prolaktina, DHEA v krvi in 17-CS v urinu ostaja v mejah normale. Razmerje LH/FSH se je povečalo za 3-4 krat. Pri hormonsko odvisnih tumorjih jajčnikov se raven testosterona in prolaktina v krvi znatno poveča.

Za mešano obliko bolezni je značilno rahlo zvišanje ravni testosterona, LH, DHEA-S v krvi in 17-KS v urinu. Koncentracija prolaktina je normalna, estradiol in FSH pa sta zmanjšana. Razmerje LH/FSH je 3,2.
Za določitev primarnega vzroka hiperandrogenizma se izvajajo testi z deksametazonom in horionskim gonadotropinom. Pozitiven rezultat HCG testa potrjuje policistično bolezen jajčnikov, ki povzroča hormonsko neravnovesje. Negativni odgovor kaže na nadledvično naravo hiperandrogenizma.

Abrahamov test razkrije bolezen nadledvične geneze, z uvedbo sintetičnih glukokortikoidov se zavira sinteza ACTH v sprednji hipofizi, kar ustavi stimulacijo skorje nadledvične žleze. Če je rezultat pozitiven, gre za hiperandrogenizem nadledvične žleze, negativni odziv je lahko znak tumorja skorje.
Poleg tega se opravi ultrazvočni pregled jajčnikov, da se ugotovijo ciste, spremembe v velikosti in strukturi organa. Če sumite na hipofizo, so indicirani elektroencefalografija, MRI, CT možganov.
Metode zdravljenja
Terapija je predpisana za vsakega bolnika posebej. Zaviralci androgenskih receptorjev zmanjšajo učinek moških hormonov na kožo, jajčnike (Flutamid, Spironolactone). Zaviralci izločanja androgenov zavirajo proizvodnjo testosterona v endokrinih žlezah (ciproteron acetat). Ta sredstva obnavljajo ravnovesje hormonov, odpravljajo simptome patologije.
Nadledvični hiperandrogenizem se kompenzira z glukokortikoidi, ki zavirajo presežek androgenov. Ženskam predpisujejo deksametazon, prednizolon in jih jemljejo med nosečnostjo, če ima bodoča mati povišana raven testosterona. Še posebej pomembno je pravočasno zdravljenje deklet, ki imajo bližnje sorodnike s prirojenim androgenitalnim sindromom. Odmerjanje in trajanje zdravila predpiše zdravnik.

Hormonsko zdravljenje hiperandrogenizma se izvaja z glukokortikosteroidi v kombinaciji peroralnih kontraceptivov(Diane-35), agonisti GnRH. Blagi hiperandrogenizem se zdravi s takšnimi zdravili. geneza jajčnikov, PCOS.
Zdravljenje brez zdravil
Za vzpostavitev hormonskega ravnovesja ženskam svetujemo, da redno vadijo zmerno telesna aktivnost, opusti slabe navade, vodi zdrava slikaživljenje. Pomembno je, da se držite diete, naredite uravnoteženo prehrano, ki izključuje kavo, alkohol, ogljikove hidrate, živalske maščobe. Koristno je jesti sveže sadje, zelenjavo, mlečni izdelki, prehransko meso in ribe. Za nadomestitev pomanjkanja vitaminov se uporabljajo farmacevtski pripravki.

Zdravljenje ljudska zdravila se lahko izvaja le v povezavi z glavno terapijo. Najprej se morate posvetovati z zdravnikom.
Hiperandrogenizem povzroča motnje v delovanju številnih organov in sistemov, vodi do razvoja insuficience nadledvične žleze in jajčnikov, neplodnosti, sladkorne bolezni tipa 2. Za preprečevanje pojava simptomov hirzutizma, kožnih izpuščajev, metaboličnega sindroma je indicirano hormonsko zdravljenje.
Bibliografija
- Kozlova V.I., Puchner A.F. Virusne, klamidijske in mikoplazmozne bolezni genitalij. Vodnik za zdravnike. Sankt Peterburg 2000.-574 str.
- spontani splav, okužba, prirojena imunost; Makarov O.V., Bakhareva I.V. (Gankovskaya L.V., Gankovskaya O.A., Kovalchuk L.V.) - "GEOTAR - Media." - Moskva. - 73 str. - 2007.
- Nujna stanja v porodništvu in ginekologiji: diagnoza in zdravljenje. Pearlman M., Tintinally J. 2008 Založnik: Binom. Laboratorij znanja.
- L.V. Adamyan in druge malformacije maternice in nožnice. - M .: Medicina, 1998.
Hiperandrogenizem mešane geneze se lahko kaže z znaki jajčnikov in nadledvične oblike bolezni. Za vsako žensko v rodni dobi je ena najbolj neprijetnih bolezni. To bolezen najdemo pri 4-6% žensk v rodni dobi. Med glavnimi vzroki za to težavo je treba omeniti presežek moških hormonov in intenzivno telesno aktivnost.
Simptomi hiperandrogenizma jajčnikov
Glavni simptomi te bolezni vključujejo kozmetične manifestacije - akne, izpadanje las in hirzutizem. Poleg tega ima lahko hiperandrogenizem tudi ginekološke manifestacije. Zelo pogosto imajo ženske, ki trpijo za to boleznijo, menstrualne nepravilnosti in sindrom policističnih jajčnikov. Drug neprijeten ginekološki simptom je neplodnost. Omeniti velja tudi, da so lahko debelost, diabetes mellitus, dislipidemija in manifestacija znakov moških hormonov simptom te bolezni. Ti znaki vključujejo:
- rast dlak na obrazu;
- spreminjanje tembra glasu;
- razširitev ramen.
Diagnostika
Lahko se diagnosticira celo blago hiperandrogenizem jajčnikov. Zato se morajo ženske, ki se soočajo z zgornjimi simptomi, vsekakor obrniti na specializirane strokovnjake. Diagnoza te bolezni običajno temelji na podatkih ultrazvoka, hormonskih in kliničnih preiskav. Bolnice, ki trpijo za hiperandrogenizmom jajčnikov, imajo praviloma povečan indeks telesne mase in število hirsute 15,2 ± 0,6. Tudi med diagnostičnim pregledom prisotnost visoka koncentracija testosteron, luteinizirajoči in folikle stimulirajoči hormoni. Na ultrazvoku se lahko pojavi povečanje volumna jajčnikov in stromalna hiperplazija.
Zdravljenje patologije
Zdravljenje hiperandrogenizma jajčnikov mora predpisati izključno specialist. Način zdravljenja je neposredno odvisen od ciljev bolnika. Če namerava v prihodnosti spočeti otroke, se za zdravljenje najpogosteje uporablja klomifen. V primeru, da bolnik ne bo obnovil plodnosti, bo zdravnik verjetno predpisal peroralno kontracepcijo. Zaradi tega se bo raven testosterona in androstendiona pri bolniku znatno zmanjšala. Alternativa temu zdravljenju je jemanje spironolaktona. Tudi za zdravljenje te patologije se lahko uporabi kirurška metoda - kirurška odstranitev jajčnikov.
Blaga hiperandrogenizem jajčnikov, PCOS se odzivajo na hormonsko zdravljenje z glukokortikosteroidi, kombiniranimi peroralnimi kontraceptivi, agonisti GnRH.
Kaj je hiperandrogenizem nadledvične žleze
Virilizacija nadledvične geneze se kaže z razvojem adrenogenitalnega sindroma (AGS) - kot posledica prirojene disfunkcije nadledvične skorje. Je genetsko pogojena motnja, podedovana avtosomno recesivno. AGS je razložen z inferiornostjo encimskih sistemov v žlezi: pri 80-90% bolnikov se manjvrednost kaže s pomanjkanjem C21-hidroksilaze.
Patogeneza (kaj se zgodi?) Med hiperandrogenizmom nadledvične žleze
Glavni patogenetski mehanizem AGS je prirojena pomanjkljivost encima C21-hidroksilaze, ki sodeluje pri sintezi androgenov v skorji nadledvične žleze. Tvorbo C21 hidroksilaze zagotavlja gen, ki se nahaja v kratkem kraku enega od 6. para kromosomov. Patologija se morda ne kaže, če je en patološki gen podedovan in se kaže v prisotnosti okvarjenih genov v obeh avtosomih 6. para. Delna blokada sinteze steroidov pri prirojenem pomanjkanju C21-hidroksilaze poveča sintezo androgena.
Do določene starosti se nadomesti blago pomanjkanje C21-hidroksilaze v nadledvičnih žlezah. S povečanjem delovanja nadledvične žleze (čustveni stres, začetek spolne aktivnosti, nosečnost) se moti sinteza steroidov v smeri hiperandrogenizma, ki posledično zavira sproščanje gonadotropinov in moti ciklične spremembe v jajčnikih.
V tem primeru je v jajčnikih možno naslednje:
- zaviranje rasti in zorenja foliklov na zgodnjih fazah folikulogeneza, ki vodi do amenoreje;
- zaviranje rasti, zorenja folikla in jajčeca, ki ne more ovulirati, kar se kaže z anovulacijo in oligomenorejo;
- ovulacija z okvarjenim rumenim telesom: kljub redni menstruaciji pride do insuficience lutealne faze cikla.
Pri vseh teh variantah hipofunkcije jajčnikov pride do neplodnosti. Pogostost spontanih splavov z AHS doseže 26%.
Simptomi hiperandrogenizma nadledvične žleze
Odvisno od resnosti pomanjkanja C21-hidroksilaze in s tem hiperandrogenizma ločimo klasično obliko AHS in pljuč ali pozne (pubertetne in postpubertalne) oblike AHS.
Klasično obliko AGS spremlja prirojena nadledvična hiperplazija. Takšna virilizacija vodi v patologijo zunanjih spolnih organov (lažni ženski hermafroditizem) in napačno določitev spola ob rojstvu. Otroci s takšno patologijo opravijo kirurško korekcijo iole, nadaljnje zdravljenje in opazovanje izvaja pediatrični endokrinolog.
V puberteti so glavne pritožbe bolnikov hirzutizem, akne, neredna menstruacija. Menarha se začne pri 15-16 letih, nato je menstruacija neredna, obstaja nagnjenost k oligomenoreji. V tem obdobju je hirzutizem bolj izrazit: rast dlak vzdolž bele črte trebuha, na zgornji ustnici, notranji strani stegen. Koža je mastna, porozna, z več aknami, obsežnimi madeži hiperpigmentacije. V telesni postavi je opazen tudi vpliv androgenov: blage moške poteze s širokimi rameni in ozko medenico, skrajšanje okončin, nizka rast. Po nastopu hirzutizma so mlečne žleze hipoplastične.
Pri bolnicah z jostpubertetno AHS so menstrualne in reproduktivne funkcije motene. Postpubertetna oblika AHS se kaže kot zgodnja prekinitev nosečnosti. Resnost reproduktivnih motenj je odvisna od stopnje pomanjkanja C21-hidroksilaze: od zmanjšanja reproduktivne funkcije zaradi anovulacijskih ciklov do spontanega splava zaradi nastanka okvarjenega rumenega telesa. Hirzutizem je rahlo izražen: redka rast dlak na beli črti trebuha, posamezne dlake nad zgornjo ustnico. Postava je ženska, mlečne žleze so precej razvite, presnovne motnje so netipične.
Diagnostika hiperandrogenizma nadledvične žleze
Pri spraševanju odkrijejo menstrualne nepravilnosti pri sestrah in sorodnikih pacientke po materini in očetovi strani. Pri AGS se prekomerna spolna rast las razvije zgodaj in hitro, menarha nastopi pozno in menstruacija je v prihodnosti neredna.
Za AGS so atletska postava, hipertrihoza, akne, zmerna hipoplazija mlečnih žlez patognomonične. AGS ne spremlja povečanje telesne mase, za razliko od drugih endokrinih motenj s hipertrihozo.
Glavna vloga pri diagnozi AHS pripada hormonskim študijam. Za pojasnitev izvora androgenov se pred in po testu deksametazona opravijo hormonske študije. Zmanjšanje ravni 17-KC v urinu, testosterona in dehidroepiandrosterona v krvi po jemanju zdravil, ki zavirajo sproščanje ACTH, kaže na nadledvični izvor androgenov.
Diagnoza postpubertetne hipertenzije temelji na:
- hipertrihoza in zmanjšana reproduktivna funkcija pri pacientovih sestrah po materi in očetu;
- pozna menarha (14-16 let);
- hipertrihoza in neredne menstruacije iz obdobja menarhe;
- virilne značilnosti morfotipa;
- povečanje vsebnosti 17-KC v urinu, testosterona in dehidroepiandrosterona v krvi ter znižanje njihove ravni na normalno po jemanju deksametazona.
Podatki ultrazvoka jajčnikov kažejo na anovulacijo: folikli različne zrelosti ne dosežejo predovulacijske velikosti. Bazalna temperatura z raztegnjeno prvo in skrajšano drugo fazo kaže na insuficienco rumenega telesa, vrsta vaginalnih brisov je androgena.
Zdravljenje hiperandrogenizma nadledvične žleze
Izbira zdravil pri bolnicah z AHS je določen cilj terapije: normalizacija menstrualnega ciklusa, stimulacija ovulacije, supresija hipertrihoze.
Za odpravo motenj hormonske funkcije skorje nadledvične žleze se uporabljajo glukokortikosteroidna zdravila. Odmerek deksametazona se določi glede na raven 17-KC v urinu, dehidroepiandrosterona in testosterona v krvi (med zdravljenjem raven teh hormonov ne sme presegati zgornje meje norme). Učinkovitost zdravljenja poleg hormonskih študij spremljamo z merjenjem bazalne temperature in spremljanjem menstrualnega ciklusa. Z nepopolno drugo fazo menstrualnega cikla je treba stimulirati ovulacijo od 5. do 9. dne, v ozadju katere pogosto nastopi nosečnost. Da bi se izognili spontanemu splavu, je treba zdravljenje z glukokortikosteroidi nadaljevati, njegovo trajanje se določi individualno.
Če ženska nosečnost ne zanima in je glavna pritožba hipertrihoza in pustularni kožni izpuščaji, se priporočajo pripravki, ki vsebujejo estrogene in antiandrogene. Diana učinkovito vpliva na hipertrihozo, zlasti v kombinaciji z androkurjem v prvih 10-12 dneh. Diana se predpisuje od 5. do 25. dneva menstrualnega ciklusa 4-6 mesecev.
Antiandrogeni učinek daje verospiron, ki je posledica zatiranja tvorbe dihidrotestosterona iz testosterona v koži, lasnih mešičkov in žleze lojnice... Veroshpiron je predpisan 25 mg 2-krat na dan. Uporaba veroshpirona 4-6 mesecev zmanjša raven testosterona za 80%, vendar ni bilo znižanja ravni kortikotropnih in gonadotropnih hormonov.
Uporaba sintetičnih progestinov zmanjšuje tudi hipertrihozo, vendar uporaba teh zdravil pri ženskah z AHS ne sme biti dolgotrajna, saj je supresija gonadotropinov nezaželena v primeru zatiranja delovanja jajčnikov.
Na katere zdravnike se morate obrniti, če imate hiperandrogenizem nadledvične žleze?
ginekolog
Promocije in posebne ponudbe
Medicinske novice
12., 13. in 14. oktobra v Rusiji poteka obsežna družabna akcija za brezplačne preiskave strjevanja krvi - "Dan INR". Akcija je tempirana na Svetovni dan boj proti trombozi.
07.05.2019
Incidenca meningokokne okužbe v Ruski federaciji se je v letu 2018 (v primerjavi z letom 2017) povečala za 10 % (1). Eden najpogostejših načinov preprečevanja nalezljivih bolezni je cepljenje. Sodobna konjugirana cepiva so namenjena preprečevanju pojava meningokokne okužbe in meningokoknega meningitisa pri otrocih (tudi zelo zgodnja starost), mladostniki in odrasli.
25.04.2019
Prihaja dolg vikend in mnogi Rusi bodo šli počivat izven mesta. Ne bo odveč vedeti, kako se zaščititi pred ugrizi klopov. Temperaturni režim maja spodbuja aktivacijo nevarnih žuželk ...
Virusi ne lebdijo v zraku, ampak lahko pridejo tudi na ograje, sedeže in druge površine, pri tem pa ostanejo aktivni. Zato je na potovanjih ali javnih mestih priporočljivo ne le izključiti komunikacijo z ljudmi okoli, ampak se tudi izogibati ...
Vrnite si dober vid in se za vedno poslovite od očal in kontaktne leče- sanje mnogih ljudi. Zdaj ga je mogoče hitro in varno uresničiti. Nove priložnosti laserska korekcija vid se odpre s popolnoma brezkontaktno tehniko Femto-LASIK.