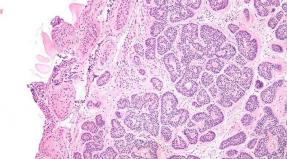
Immunohistokeemia (IHG analüüs) rinna. Pehme koevähi immunohistokeemiline uuring immunohistokeemiline uuring
Tuumorihariduse kahtlustatavuses näeb patsient ette mitmeid standardseid uuringuid.
Pahaloomulise kahjustuse diagnoosimine võib kokku puutuda ainult biopate - immunohistokeemilise uuringu (IHD) muutuste hindamise põhjal peetakse üheks kõige usaldusväärsemaks kasvajarakkude tuvastamiseks.
Mis on immunohistokeemiline uuring?
Immunohistokeemilise uuringu olemus on bioloogilise materjali proovide mikroskoobi uuring, st biopsia poolt saadud kudede.
Pre-koe töödeldakse teatud spetsiifiliste antikehadega.
Ja vähirakud ise on põhjaliku uuringu objektid mitu aastakümmet.
Nende uuringute käigus õnnestus teadlased kindlaks teha, et kasvajarakud toodavad spetsiifilisi valke või helistavad neile antigeene.
Nendel valkudel on võime seonduda antikehadega. See oli see, et IGI põhimõte oli ehitatud - patsiendi terava kanga uuringute töötlemiseks töödeldakse mitmete standardsete antikehade ja uuringu all mikroskoobi viiakse läbi.
Kui antikehad suhtlevad vähirakkudega suhtlemises, on neil fluorestsentsi vara, st seal on kuma, mida iseloomustavad erinevad lainepikkused. See tähendab, et kui avastatud biopate sarnane muutus tuvastatakse, siis saate juba pahaloomulise hariduse seada suurema tõenäosusega.
Täna on antikehad välja töötatud ja aktiivselt kasutatavad enamiku kõige levinumate neoplasme.
Immunohistokeemiline uuring võimaldab:
- Määrake neoplasma ja selle alamliikide tüüp.
- Primaarse vähktõve organismi puhul on tavaline.
- Määrake metastaaside allikas, kui BIOPSYTTE saadakse vähi sekundaarsest fookusest.
- Hinnates, kui efektiivne ravi patsientide OSCO-SCABERS.
- Paigaldage pahaloomuliste kasvajate etapp.
- Uurige tuumorite proliferatsiooni, st kasvab kasvaja kasvutempo.
IGH peetakse informatiivsem meetod võrreldes tundlikum histoloogiline. Kuid mõnel juhul on see vajalik täpselt histoloogia, mistõttu on soovitav kasutada mõlemat analüüsi.
Näidustused
IgG meetodit saab kasutada peaaegu iga kudede uurimiseks inimkehas. Seda tüüpi uuringud nimetatakse peamiselt siis, kui kasvajaprotsessi arendamise kahtlus on kahtlus.
Kasutatakse immunohistokeemilisi uuringuid:
- Et määrata primaarse, enamasti ühe, neoplasme.
- Metastaaside tuvastamiseks.
- Kui on vaja kindlaks määrata kasvajate arendamise ja voolu prognoosi.
- Meetodina retseptorite uurimiseks hormoonide reale.
- Lümfoproliferatiivsete riikide tüübi määramiseks.
- Mikroorganismide avastamiseks.
IGO-de suhtes ei ole vastunäidustusi. Seda analüüsi ei saa läbi viia ainult siis, kui kahjustatud kudede proovide tara tekivad vastupandamatu raskusi.
Kuidas analüüs on?
Igh toimub mitmetes etappides, esimene on dolboatood, st aiakangad analüüsimiseks.
Proov saadakse biopsia abil, mõnel juhul on endoskoopilise või kirurgilise operatsiooni läbiviimisel võimalik kudede või nende kõrvaldamise korral vajutada.
Kuidas saadakse bioloogiline materjalSõltub neoplasma lokaliseerimisest ja selle tüübist. Kokkupandav materjal asetatakse formaliinini ja alles pärast seda saadetakse need laborikeskusesse.
Laboratooriumis on kanga proov mitmete muudatustega:
- Materjal on hammustada ja valatakse parafiiniga. Seega saadakse histoloogilised plokid, need on võimalik neid igavesti salvestada, seetõttu võib Igh-i vajadusel korrata.
- Järgmine etapp Microtoming on saada parimaid sektsioone laiusega kuni 1,0 μm parafiinplokkidest. Viilud jaotatakse spetsiaalsetele prillidele.
- Saadud osad värvitakse immunohistokeemiliste preparaatidega, st antikehade lahused teatud kontsentratsioonis. Väike paneeli saab kasutada õppimiseks - see sisaldab 5 tüüpi antikehi. Suur paneel sisaldab 6 kümneid markereid. Millised antikehad kasvajarakkudega interaktsiooni sisenevad, sõltub väidetava neoplasma tüübist.
Tulemused IGH on muutumas tuntud 7-15 päeva.
Igh rinnavähiga
 Teatavate immunohistokeemiliste markerite määramiseks saadi. Pahaloomulise hariduse kahtlustatavuses olla kindlasti selliste retseptorite arv östrogeeni ja progesterooni puhul.
Teatavate immunohistokeemiliste markerite määramiseks saadi. Pahaloomulise hariduse kahtlustatavuses olla kindlasti selliste retseptorite arv östrogeeni ja progesterooni puhul.
Nende hormoonide liigne ületamine tekitab pahaloomulise hariduse kasvu ja mõjutab metastaaside välimust. Ighs ekspressiooni progesterooni ja östrogeeni, mis võimaldavad täpsemaid kehtestada haiguse etapp ja välja selgitada, kas hormonaalne ravi on näidatud antud juhul.
Kasvajate S. kõrge kontsentratsioon Enamikku hormoonidest ei ole enamasti eristatud suurenenud aktiivsusega ja neid töödeldakse edukalt antmonaalsete ravimitega.
Juhtimisel Igh on vaja sellist indikaatorit määrata Ki-67, see näitab protsessi pahaloomulist kasvamist. Kui Ki-67 rinnavähi rambles ainult 15%, peetakse haiguse tulemust soodsaks.
30% tasemel räägivad nad kasvaja arengu kiirest kiirust, selle kasvu lõpetamine toimub kemoteraapia mõju all. Kui indikaator on alla 30%, teostab patsientide ravi hormonaalsete vahenditega.
Patsientide uurimine võimaldas kindlaks teha, et kui KI-67 on alla 10%, ellujäämishindade lähenemisviis 95%. Selle näitaja tasandil täheldatakse 90% -l peaaegu sada protsenti surmavat tulemust.
Immunohistokeemilised uuringud nimetatakse mitte ainult pahaloomulise kahjustusega rinnale, see uuring on informatiivne:
- Viljatus.
- Reproduktiivse funktsiooni patoloogilised muutused.
Endomeetria
Endomeetriumi kudede immunohistokeemiline uuring on määratud:
- Viljatusega.
- Sagedase mitte-ebaselge raseduse.
- Mitme ebaõnnestunud katsete patsientidel Eco.
- Diagnoosimine krooniline vorm Endomeetriumi.
Igh võimaldab teil kindlaks teha, kas on rakke, mis takistavad kontseptsiooni. See analüüs määrab samaaegselt, kuidas patoloogia tuvastamise korral on emaka koe retseptorid reageerima hormonaalse stimulatsiooni jaoks, näitab see endomeetriumi-endomeetriidi, hüperplaasia, endomeetriumi diferentseerimisprotsessi desünkroniseerimise muutusi.
Sellised rikkumised on kahel juhul kolmest muutumisest kontseptsioonide ja töötleva tööriistade probleemide peamiseks põhjuseks.
Endomeetriumi kangad, sõltuvalt tuvastatud patoloogiast viiakse läbi tsükli erinevatel päevadel, peab biopsia päev määrama arsti. Ma saan installida vähihaigus ja mitme alamliikide HPV infektsioon.
Dekodeerimistulemused
Koostatud proovide uurimine patoloogi poolt, peab tal olema IGH-meetodi testide erilise ettevalmistamise sertifikaat.
Kokkuvõttes määratakse kindlaks antikehade näitajad, mille suhtes määratakse uuringu all oleva materjali patus.
Koe morfoloogiline struktuur on tingimata näidatud, st atüüpiliste rakkude tüüp ja nende arv.
Teatavate antigeenide identifitseerimine näitab vähipatoloogia tüüpi. Kuid tuleb meeles pidada, et diagnoosimine on eksponeeritud ainult nende diagnostiliste protseduuride kogu osas. Tõlgendage IGH-i tulemused onkoloogi tulemused.
Uurimishind
Immunohistokeemiliste uuringute maksumus sõltub sellest, kui palju antikehi kasutatakse analüüsimisel.
Standardne uuring (2 ja kuni 5 antikeha) enamikus kliinikus on 4-5 tuhat rubla. Kui tosin antigeenid ilmuvad kohe, siis võib maksumus olla palju kõrgem - 15 000 rubla.
Video selle kohta, kuidas immunohistokeemia aitab diagnoosida pahaloomulise kasvaja:
Immunohistokeemiline (Igh) uuring on meetod pahaloomuliste kasvajate spetsiifiliste antigeensete omaduste tuvastamiseks. Kasutatakse selleks, et tuvastada raku- või koekomponendi (antigeeni) lokaliseerimise in situ, sidudes selle märgistatud antikehadega ja lahutamatu osa kaasaegne diagnoos Vähk, pakkudes lokaliseerimistuvastuse erinevate rakkude, hormoonide ja nende retseptorite, ensüümide, immunoglobuliinide, rakukomponentide ja individuaalsete geenide kudedes.
IgG-uuringute eesmärgid
Igh-uuringud võimaldavad:
1) teostada kasvajate histogeneetilist diagnoosi;
2) määrata neoplasma nosoloogiline versioon;
3) tuvastada esmane kasvaja metastaasis tundmatu primaarse põisakuga;
4) määrab kasvajahaiguse prognoos;
5) määrata kindlaks rakkude pahaloomuline transformatsioon;
6) määravad võimalused;
7) tuvastada nii kasvajarakkude takistus kui ka tundlikkus kemoterapeutiliste preparaatide suhtes;
8) määrab kindlaks kasvajarakkude tundlikkus kiirguse raviks.
Kuidas IgG-uuringud on?
IgG uuringud algavad materjali taraga. Selleks viiakse nad läbi, kus kasvaja kasvaja ja lähedal asuvad kuded võetakse ära või materjal pärineb operatsioonist. Seejärel on materjal fikseeritud. Pärast kinnitamist saadetakse materjal juhtmestikule, mis võimaldab teil valmistada seda tööks (rasvatustamine ja parandamine). Pärast juhtmestikud valatakse kõik proovid parafiiniga, saada histoloogilisi plokke. Parafiinplokid salvestatakse igavesti, nii et saate teostada IGH-uuringuid varem tehtud parafiinplokkide juuresolekul.
Järgmine etapp IgG uuringud on mikrotomiline - laboratoorselt teeb kärped parafiinplokkide paksus kuni 1,0 mikronit ja asetab need erilistele histoloogilistele klaasidele.
Siis on järjekindlalt rutiinne maalimis- ja immunohistokeemiline uuring, mis võimaldab igal etapil üha enam eristada fenotüübi ja tuumori nosomeeni.
Nagu näete, on Igh-uuringud keeruline mitmeastmeline protsess ja seetõttu peaksid igh-uuringud valima kõige rohkem kaasaegse laboratooriumi kõrgelt kvalifitseeritud spetsialistide ja suur osa automatiseerimisest - nii vähendate halva kvaliteediga diagnostika saamise riske. Selline labor täna on noor.
Eraldi tuleb öelda selle uuringu ajastamise kohta. Keskmiselt Venemaal teostatakse IGH-uurimist ajas 10 päeva kuni mitu nädalat. Kui teiega ühendust võtta, saate IgG uurimist teha vaid 3 päeva jooksul! Samuti on Igh-uuringute rakendamise eelise Yunimas on teie materjalid Venemaa linna uuringus. Vajadusel kontrollige, esitades teadusuuringute taotlus või helistaja Hotline (Venemaal tasuta): 8 800 555 92 67.
Määratlusmeetod BioPtate histoloogiline uurimine vastavalt Maailma Terviseorganisatsiooni (WHO) histoloogilise klassifikatsioonile, millel on värvimise hematoksüliin-eosiin. IHG uuring, kasutades koepetsiifiliste ja prognostiliste antikehade spektrit (kuni viie antikeha) (peroksidaasi ja avidiin-biotiini meetodid).
Uuringu all olev materjal Vaadake kirjeldust
Kättesaadav lahkumine maja juurde
Mitmesuguste lokaalsete biopsia metastaatiliste kujutluste põhjalik uuring, sealhulgas morfoloogiline kirjeldus ja kudede markerite ekspressiooni ekspressiooni hindamine, et määrata primaarse kasvaja fookuse histogeneesi.
Statistika kohaselt 3-15% juhtudest pahaloomulised kasvajad Ilmselge metastaasidega. Metastaasid ilma avastatud esmase tähelepanuta iseloomustab juhuslik, ebatüüpiline lokaliseerimine ja kiire progresseerumise protsessi. Kahjustuse kolme ja rohkem metastaatilise kahjustusega patsientide keskmine eluiga on kolm kuud. Samal ajal tuvastatakse esmase fookuse lokaliseerimine 60-70% patsientidest ainult autopsile. Õigeaegne diagnoosi määrab ravi taktika enne esmase põisa avastamist.
Patomorfoloogiline diagnoosi metastaaside talumatud kasvajad näevad ette oma morfoloogilise tüübi määratluse, selgitades tõenäolise metastaaside allika, pahaloomulise potentsiaali hindamise. Esimene ülesanne on lahendada biopsia materjali rutiinse histoloogilise uurimisega (värvimine hematoksüliin-eosiiniga), teine \u200b\u200b- spetsiaalsete uurimismeetodite rakendamine: histokeemiline, immunohistokeemiline (igh) või molekulaarne geneetiline meetod kala (paelukus in situ hübridisatsioon).
Rutiinse morfoloogilise diagnostikaga, metastaatiliste kasvajatega vastavalt soovitustele Euroopa ühiskond Meditsiiniline onkoloogia ESMO (Euroopa Medical Onkoloogia ühiskond) (2004) on jagatud viie olulise kategooria: adenokartsinoomi, lamedate rakkude vähi, neuroendokriinvähi, diferentseerumata vähi, diferentseerimata kasvaja. Need morfoloogilised kategooriad koos protsessi levimuse andmetega võimaldab paljudel juhtudel määrata piisava ülevaatuse kava (ja ravi). Niisiis, näiteks, kui see identifitseeritakse lamedat belling vähi metastaasiga emakakaela lümfisõlmed Endoskoopiline uurimine ülemiste hingamisteede ja seedetrakti organite on vajalik. IHG uuring, sõltuvalt neoplasma morfoloogilisest liigist, võimaldab teil selgitada kasvaja histogeneesi ja / või määrata esmase sulgemise tõenäolise lokaliseerimise.
IHG teadusuuringute esmaste kasvajate ja nende metastaaside kasutatakse lai spektri Kude-spetsiifilised markerid: -Citospecific (leukotsüütide diferentseerumise klastrid (diferentseerumise klastrid), silelihase aktiin, moglobiin, türeglobuliin); -Margers levuti (Ki67, PCNA - prolifertititini raku tuumantigeen); - Kasvaja markerid - onkofetaalsed antigeenid (fetoproteiin, kartsinomeetriumi antigeen); -GGURONID (östrogeen, progesteroon); -Ferminesiinid, rakkude valkude tooteid jne.
Unified algoritmid igh uuringute metastaaside kasvajad ilma rafineerimata primaarse äraolekuta ei ole arenenud. Kasvajarakkude diferentseerumise suunda ja mitmete bioloogiliste kasvajaparameetrite õige määramine iseenesest on teatavate teraapia mustrite määramise tähis. Näiteks adenokartsinoomi metastaaside avastamine amorinaarse piirkonna amphosalsis võivad tähendada sobiva etapi rinnavähi ravis sarnase ravi ravi. Ekspressiooni avastamine östrogeeni retseptorite ja progesterooni ekspressiooni sellises adenokartsinoomi võib märkida, et nimetada humon-ravi, sõltumata olemasolu kindlaksmääratud kasvaja sõlme rinnaga. Erineva diagnostika kasutamiseks soovitatav algoritmi näide.
Teadusuuringute materjal: kasvaja bioptat, fikseeritud parafiiniplokis.
Kirjandus
- Blaszyk H., Hartmann A., Bjornson J. Tundmatu Primaarse vähk: kliinopatoloogilised korrelatsioonid. APMIS. 2003; 111 (12): 1089-1094.
- DABBS D.J. Diagnostiline immunohistokeemia: theranostic ja genoomse rakendused. Elsevier, 4-th väljaanne. 2013: 960.
- Di Patre P.L., Carter D. Sternbergi diagnostika kirurgilise patoloogia ülevaade. Wolters Kluver, 2-ND väljaanne. 2015: 488.
- Dieet M., Wittigind S., Bussolati G., von Winterfeld M. Patoloogiliste eksemplari eeltüüp onkoloogias. Sringer. 2015: 133.
- Dodd L.G, Bui M.M. Pehmete kudede ja luu patoloogia atlas. Demosmedical. 2014: 720.
- EDGE S.B, BYRD D.R., COMPTON C.C., Fritz AG. Sringer, 7-th väljaanne. 2011: 646.
- Vanem D.E. Hoova "S naha histopatoloogia. Vanad Kluver, 11-väljaanne. 2014: 1544.
- Epstein J., Netto G. Biopsia eesnäärme tõlgendamine. Lippincott Williams ja Wilkins, 5-th väljaanne. 2014: 450.
- Erickson L. Atlas endokriinse patoloogia. Sringer, 1-st väljaanne. 2014: 178.
- ESMO Kliinilised soovitused tundmatu primaarse saidi vähi diagnoosimiseks, raviks ja järelkontrollimiseks. Annals onkoloogia. 2005; 16 (S.1): 175-176.
- Fletcher C.M., Bridge J.A., Hogendoorn P., Mertens F. Kes klassifitseerimine kasvajate pehme koe ja luu. Kes vajuta, 4-th väljaanne. 2013; 5: 427.
- Kurman R.J., Carcangiu M.L., Herrington C.S., noor R.h. WHO naissoost reproduktiivorganite kasvajate liigitamine. Kes vajuta, 4-th väljaanne. 2014; 4: 316.
- Louis D.n., Ohgaki H., Wiestler O.d., Cavenee W.K. Kes klassifitseeritakse kesknärvisüsteemi kasvajate klassifikatsioon. Kes vajuta, 4-th väljaanne. 2007; 1: 312.
- Malpica A., E. E. E.D. Emaka emakakaela ja korpuse biopsia tõlgendamine. Wolters Kluver, 2-ND väljaanne. 2015: 368.
- Nishizuka S., Chen S.T., Gwadry F. et al. Diagnostilised markerid, mis eristavad käärsoole ja munasarjade adenokartsinoomid: genoomse, proteoomilise ja koe massiivi profiilide identifitseerimine. Vähiuuringud. 2003; 63: 5243-5250.
- NORDI Q.C. http://www.nordiqc.org.
Standardiseeritud immunohistokeemiline uuring: retseptori staatus rinnavähiga (PR, ER, KI67, HER2 Neu). See viiakse läbi ainult valmis mikrodigaratsiooni juuresolekul slaidil ja koeproovil parafiinühikus.
Vene sünonüümid
IHG uuringus (RE, RP, HER2 / NEU, Ki-67), rinnavähi retseptori staatuse immunohistokeemiline analüüs.
Sünonüümid Inglise
IHC (immunohistokeemia) test rinnavähi retseptori staatuse (ER, PR, HER2, KI67), HER2 üleekspressioon IHC, östrogeeniretseptorite, progesterooniretseptorite, ER ja PR staatuse, östrogeeni ja progesterooni retseptori staatus.
Uurimismeetod
Immunohistokeemiline meetod.
Millist biomaterjali saab uurimiseks kasutada?
Parafiiniplokk Bioplatomi moodustumisega rinnaga. Esmane kasvajakoe saab saada paksu biopsia abil ning sisselõike ja ekstsisiooni kirurgiliste sekkumiste abil. Metastaaside tuvastamiseks biopsia saab teha kangast seinast rindpiirkondlikud lümfisõlmed või kaugorganid.
Üldteave
Kaasaegsed põhimõtted ja strateegiad rinnavähi raviks põhinevad muu hulgas retseptori staatuse hindamise tulemuste ja kasvajarakkude proliferatsioonipotentsiaali tulemuste kohta. Kasvajarakkudel on võime valmistada ja asetada spetsiaalsete valkude oma pinnal - retseptoritel, mille stimulatsioon põhjustab mobiilse jagunemise ja kasvaja kasvu käivitamiseni. Sellised retseptorid suudavad seonduda organismis olevate ainetega tavaliselt ja esialgu mitte mingil juhul seotud pahaloomuliste kasvajate arendamisega. Vastavalt asjakohasele kliinilised soovitusedRinnavähi puhul järgmiste retseptorite olemasolu järgnevate retseptorite kasvajarakkudes, millest erinevad kombinatsioonid nimetatakse retseptori olekuks:
Hormoonide retseptorid - östrogeenid ja progesteroon ( Er,PR.). Oluline osa rindade kasvajatest sõltub hormonaalselt, st nende kasvu säilitatakse ja stimuleeritakse östrogeeni ja progesterooni abil. Positiivse hormonaalse retseptori staatusega kasvajad on hästi teadlikud hormoonianaloogide teraapiast (tamoksifeen), mis blokeerivad sobivate retseptoritega - nendega seostatakse, kuid ei põhjusta intratsellulaarsete protsesside aktiveerimist ja ei lase retseptorile hiljem ühendust võtta hormoon. Seega on kasvaja er ja PR-toodete uurimine võimalikuks määrata nende tundlikkuse nende ravimite suhtes.
Teine tüüpi retseptor inimese epidermaalse kasvufaktori (inimese epidermaalne kasvufaktori retseptor 2 - HER2 / Neu.). Mõnede rindade kasvajate rakkudes esineb selle retseptori valku suurenenud arendamine, mis loomuliku kasvufaktoriga ühendamine algab kasvajarakkude jagunemise. HER2-positiivse rinnavähi patsientide koguarv on 15% -lt 20% -ni. HER2 / NEU määratlus ei ole mitte ainult prognostiline väärtus (sellised kasvajad lähevad tavaliselt kiiremini ja neil on agressiivsem kliiniline areng), kuid võimaldab teil ka hinnata võimalust kasutada sihipäraseid ravimpreparaadid - monoklonaalne antikehad retseptori HER2 - trastuzumabi (Herceptin), lapatiniibi, Pertzumabi. Lisaks on HER2-positiivsed kasvajad tamoksifeeni suhtes vastupidavad.
Proliferatiivne aktiivsus on kasvajarakkude võime näitaja piiramatule jagunemisele, mis on peamine tegur kasvaja bioloogilise agressiivsusega. Jagunemisprotsessiga kaasneb teatud valkude ilmumine rakus, millest üks on Ki-67.. Seda ei toodeta rakkudes puhkamisel, mis võimaldab seda kasutada kasvaja proliferatiivse aktiivsuse markerina. Ki-67 taseme kindlaksmääramisel on oluline prognostiline väärtus, kuna vähemalt küpsete ja diferentseeritud rakkude kasvajad on suurim proliferatiivne tegevus.
Kõiki eespool nimetatud markereid saab tuvastada biopaadi või kasvaja töömaterjali immunohistokeemilises uuringus. Lõpliku parafiiniüksuse analüüsimiseks lõigatakse parimaid sektsioone spetsiaalsest mikronist, mis seejärel kinnitatakse klaaslauaga slaidide ja värvi rutiinse värvide külge, et võimaldada üksteisest ja intertsellulaarsest ainest üksteisest eristada rakke. Seejärel värvitakse klaaside kärped koos fluorestseeruvate tähistega märgistatud antikehade lahusega. Kui soovitud retseptor esineb kasvajarakkudes, on antikehad seotud sellega ja klaasi vaatamise ajal spetsiaalse mikroskoobi all näete fluorestsentsi, mis näitab katse positiivset tulemust. Lisaks, kui vaatate lõigatud, morfoloog näeb, et värvitud marker asub südamikus, rakulise aine või kesta kasvajarakkude. Antikehadega kasutatavate lahuste kogus vastab proovis uuritud markerite arvule. Fluorestsentsi aste ja rakkude osakaal, milles see on, on immunohistokeemilise analüüsi tulemuste tõlgendamine ja neid kirjeldatakse üksikasjalikumalt asjakohases osas.
Mis on uuring?
- Hormonoretseptori staatuse ja rinnavähi proliferatsiooni aste määramiseks ravi prognoosi hindamiseks ja ravikuuri hindamiseks, sealhulgas identifitseerimisnäitajate kindlakstegemiseks ravi eesmärgil.
- Hormonaalsete retseptorite avastamise tulemuste kohaselt on anti-östrogeeni kasutamise teostatavus ja retseptori HER2-sihitud anti-Her2 ravimid. Nende markerite ilmnemise puudumine väldib ilmselgelt ebatõhusa ravi määramist. Kõrge indeks Proliferatiivne tegevus, samuti retseptori staatuse negatiivsus enamasti, on märge tsütostaatiliste ravimite lisamiseks ravile.
Millal on määratud uuring?
- Histoloogiliselt kinnitatud rinnavähi juuresolekul - esmakordselt tuvastatud, korduvate ja metastaatiliste kasvajate jaoks.
Mida tulemused tähendavad?
Immunohistokeemilise määratluse tulemuste tõlgendamisel steroidhormoonide retseptori staatus(Östrogeeni ja progesterooni) rindade kasvajates tuleks hinnata mitte ainult antikehade värvitud rakkude protsent, vaid ka värvimise intensiivsus. Mõlemad parameetrid salvestatakse alred skaalal, kus positiivsete rakkude protsent on hinnanguliselt 0 kuni 5 punkti ja värvimise intensiivsus 0 kuni 3. summa kahe näitaja summa on lõplik skoor, mille kohaselt Positiivne kasvaja retseptori staatuse määratakse: 0-2 negatiivne, 3- 8 positiivset. Selle skaala koguarv 3 vastab 1-10% värvitud rakkudele ja on minimaalne positiivne tulemus, kui hormonaalse ravi eesmärk võib avaldada tõhusust.
Mõnikord määratakse retseptori olek üksnes rakkude protsentides värvitud nuklei. Sellistel juhtudel soovitab NCCN-i, et kõiki kasvajaid peetakse positiivseks, kus on rohkem kui 1% positiivsetest rakkudest.
Värvimise tõlgendamisel retseptorHER2 /neu. Ainult membraani värvimine (raku kesta värvimine), mida hinnatakse skaalal 0 kuni +3:
tulemuseks on 0 ja +1 peetakse HER2-negatiivseks;
2 - Piiride tulemus, millel on immunohistokeemiliste uuringute kohaselt võimatu hinnata HER2-NEU retseptorirakkude pinnal olevat kohalolekut, on vaja läbi viia kala või cish uuring;
3 on positiivne tulemus - HER2-HER2-siht-ravi on tõhus.
Vastavalt Püha klassifikatsioonile Gallen konsensus (2009), madala proliferatiivse tegevuse indeks loetakse ki-67 tase Vähem kui 15%, keskmine - 16-30% ja kõrge - rohkem kui 30%.
Mis võib tulemust mõjutada?
- Pakuva parafiini plokkide kvaliteet, patoloogi arstide kogemus ja kvalifikatsioon, kuna immunohistokeemiline meetod ei ole täielikult standardiseeritud ja selle tulemuste hindamine teataval määral subjektiivselt hindama.
- Uuringu tulemuste tõlgendamist tuleks läbi viia ainult vastava eriala arst, andmed teatavate nimetamise tõhususe ja asjakohasuse kohta ravimid Sõltuvalt uuringu tulemustest oleme erakordselt nõuandev ja neid võib läbi vaadata, võttes arvesse patsiendi individuaalseid omadusi.
Olulised kommentaarid
- Tänu määramata HER2 / NEU-retseptori staatusega (immunohistokeemilise uuringu 2+ tulemus on soovitatav kala või cish-uuringu täitmine, mis kõrvaldab selle retseptori kodeeriva geeni hüperaktivatsiooni. Nende uuringute puudumise korral on lubatud korduv immunohistokeemiline uuring, kuid teise kasvajakoe proovis.
- Rinnavähi retseptori staatuse hindamiseks on mitmeid kaalud laboratooriumis aruandes, mille puhul viidi läbi kasvaja positiivse hinnang selles uuringus ja positiivsete rakkude arvu kirjeldav omadus, the Rakkude värvimisstruktuuride ja rakkude morfoloogilised omadused anti.
Biopsia rinna Biopsia histoloogiline uuring
Rindade tsütoloogiline uuring
HER2 kasvaja staatuse määramine kalade kaupa
Määramine HER2 kasvaja staatuse cish
Kes nimetab uuringu?
Onkogünekoloog onkoloog, imeloog.
Kirjandus
Dana Carmen Zaha. Immunohistokeemia tähendus rinnavähi. Maailma Journal of Clinical Oncology, 2014; 5 (3): 382-392.
NCCN kliiniliste tavade juhised onkoloogias: rinnavähk. Versioon 3.2017 - 10. november 2017. Olemas saadaval aadressil www.nccn.org.
Kliiniline laboratoorse diagnostika: National Guide: 2 T. - T. I / Ed. V. V. V. MENSHIKOVA V. V. MENSHIKOVA. - m.: Goeotar Media, 2012. lk 658-660.
V. F. SEMIGZOV, R. M. Kaltuyev, V. V. SEMILZOV, G. A. A. Dashyan, T. Y. Semilazova, P. V. Krivorowto, K. S. Nikolaev. Üldised soovitused Varase rinnavähi St. Galle-2015, kohandatud eksperdid Venemaa ühiskonna oncomologistside poolt. Naissoost reproduktiivsüsteemi kasvajad, 2015; 3: 43-60.
Alternatiivsed nimetused: Ingli, Inglise: Immunohistokeemia või IHC.
Immunohistokeemiline uuring on eriline meetod kasvajahaiguste diagnoosimiseks. Sisuliselt meetod on uurida mikroskoobi kujutiste kudede eelnevalt töödeldud spetsiifiliste antikehadega.
Kasvajarakud toodavad spetsiifilisi valke (antigeene), mis võivad seonduda teatud antikehadega. Engi ajal töödeldakse kanga proovi erinevate standardsete antikehade abil ja seejärel uuris mikroskoobi all. Kasvajarakkudega seotud antikehad on fluorestsentsi omadus - võime hõõguda talade all teatud lainepikkusega. See kuma ja võimaldab teil tuvastada vähirakke.
Praegu on kõigi kasvajate suhtes praktiliselt loodud antikehad.
Immunohistokeemiliste uuringute abil:
- kasvaja liikide ja alamliikide kindlaksmääramine;
- onkoloogilise fookuse levimuse kindlaksmääramine;
- metastaaside uuringus määratakse nende allikas;
- vähktõve ravi tõhususe hindamine;
- kasvaja pahaloomuliste kasvajate määramine;
- tuleb välja proliferatiivse aktiivsuse kasvajate (millisel kiirusel nad kasvavad).
Immunohistokeemiliste uuringute näidustused
Selle meetodiga saate uurida kõiki kangaid. Peamine näide kasvaja protsessi kahtluse tegemiseks.
Järgmised lugemised on määratletud IGI jaoks:
- primaarsete tahkete (ühekordse) kasvajate immunofenotüüp;
- immunofenotüüpimise metastaasid;
- kasvaja protsessi tulemuste prognoosimise määramine;
- teadusuuringute retseptorid erinevate hormoonide suhtes;
- lümfoproliferatiivsete riikide immunofenotüüpimine;
- mikroorganismide määratlus.
Vastunäidustused
Et see meetod Teadusuuringud ei ole vastunäidustusi. Selle võimatu on võimatu ainult siis, kui ei ole võimalik saada biopsia materjali.
Kuidas immunohistokeemiline uuring
Uuring koosneb neljast etapist:
- Dollaboratori etapp, mis seisneb analüüsi piisava valimi saamisel. Uurimisriie võib saada kasutades sisselõike või ekstsisiooni biopsia, punch-biopsia (kasutades tangid) või endoskoopilise töö ajal. BioPtaadi saamise kord ja selle ettevalmistused määratakse kindlaks kasvaja tüübi ja lokaliseerimisega. Saadud kangas asetatakse formaliini 10% lahusesse ja saadetakse laborisse.
- Ettevalmistus, mille jooksul töödeldakse bioptaati, millele järgneb selle esmane uuring. Samal etapil valmistatakse parimad osad kangast.
- Värvimine lõigatud immunohistokeemiliste preparaatide, mis esindavad lahuse spetsiifiliste antikehade. Sõltuvalt sellest, kui palju erinevad tüübid Ma kasutan antikehi, eraldada väike ja suur uurimispaneel. Väikepaneel sisaldab kuni 5 antikeha, suurele - 6-ni mitmele kümnele. Tuvastatud markerite arv sõltub väidetava diagnoosi kohta.
- Värvitud proovide uurimine ja analüüs, mille järel sõlmitakse järeldus.
Uuringu tulemused muutuvad teada 7 päeva pärast (standardse uuringuga "väikese paneeli") või 15-ga (laiendatud uuring on "suurpaneel").
Tulemuste tõlgendamine

Proovide uurimine tegeleb patoloogiga, kes on IgGs eriväljaõpe läbinud. Kokkuvõttes määratakse arsti märkused, millele antikehad koe trükise (afiinsus) määratakse. Lisaks kirjeldatakse proovi morfoloogilist struktuuri - millised rakud ja millises koguses esineb.
Kude afiinsuse identifitseerimine teatud standardse kasvaja antikehade suhtes näitab konkreetset vormi onkoloogilise haiguse vormi.
Lisainformatsioon
Immunohistokeemiline uuring on praegu kasvajahaiguste diagnoosimiseks kõige täpsem meetod. See võimaldab teil panna lõpliku diagnoosi 99% täpsusega, määrake kasvaja tüüp, paljastada selle esmane lokaliseerimine.
Kirjandus:
- 21. novembri terviseministeeriumi Terviseministeeriumi korraldus "21. november 2012" arstiabi Profiiliga "patoloogiline anatoomia"
- Immunohistokeemilised meetodid: juhend. Per. alates inglise keelt Ed. G.A. Frank ja p.g. Malkova // M., 2011, - 224 lk.